我校华西药学孙逊和高分子张凌团队在Science Advances发表论文
在亚单位疫苗递送系统中取得进展
在亚单位疫苗递送系统中取得进展
近日,我校华西药学院孙逊教授及高分子科学与工程学院张凌副研究员的研究团队在ScienceAdvances杂志在线发表了题为:Theporesizeofmesoporoussilicananoparticlesregulatestheirantigendeliveryefficiency的研究论文。应用介孔氧化硅纳米粒(MSNs)作为亚单位疫苗的递送载体和佐剂,发现通过调节MSNs介孔的孔径即可调节疫苗诱导机体产生免疫应答的强度。我校华西药学院博士研究生洪小玉为该论文的第一作者,通讯作者是华西药学院孙逊教授和高分子科学与工程学院张凌副研究员。
疫苗作为控制感染性疾病最为经济有效的方式已挽救了无数生命。亚单位疫苗接种后往往需要经过以下四个级联步骤才能诱导机体产生有效的细胞免疫应答:(1)靶向淋巴结;(2)被树突状细胞摄取;(3)诱导树突状细胞成熟活化;(4)以抗原肽-MHCI分子复合物形式将抗原呈递给CD8+T细胞。这四个步骤简称为DUMPcascade。
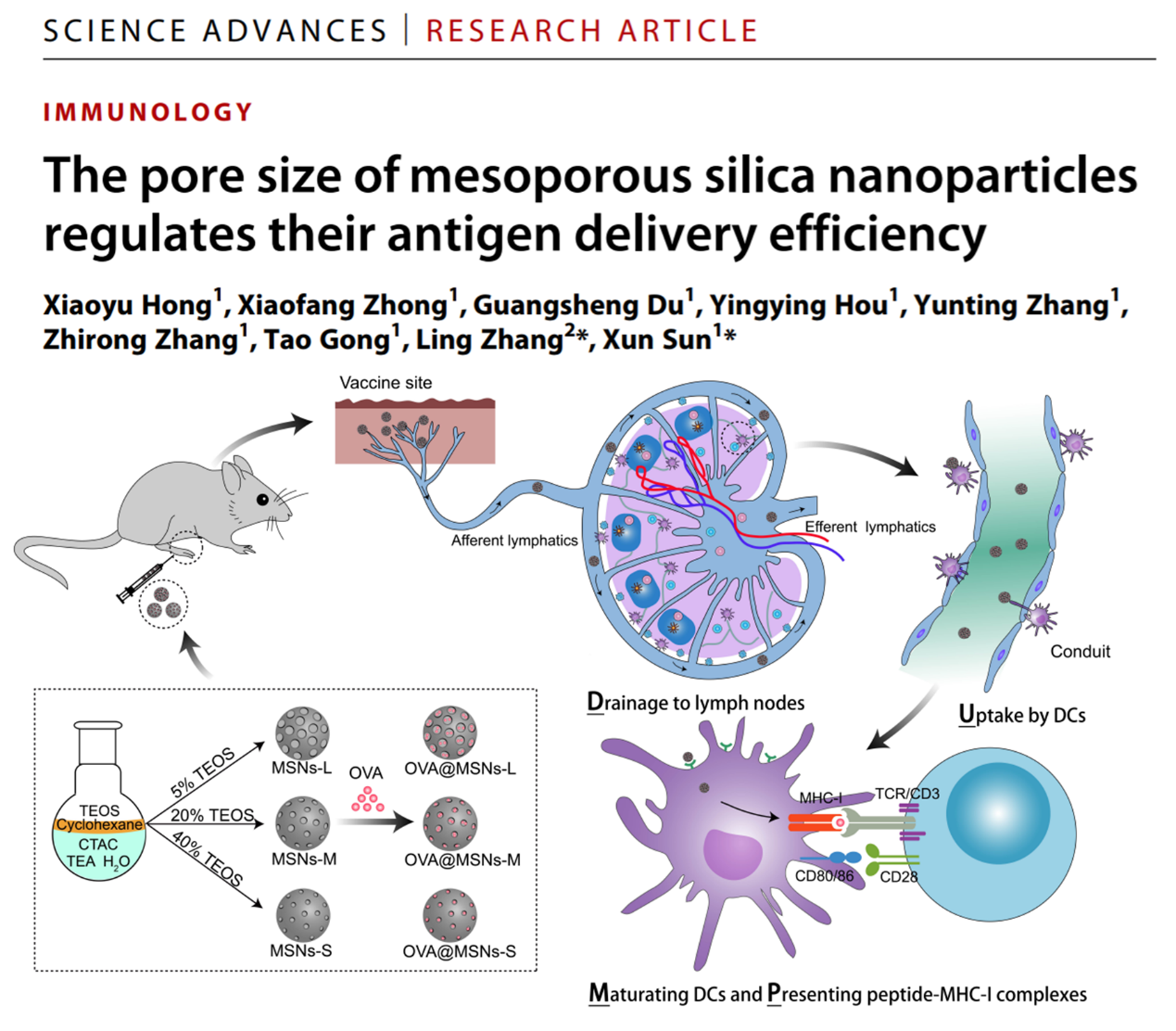
MSNs的制备及在体内诱导免疫应答的四个过程
研究人员合成了三种粒径均在85nm左右,但介孔孔径分别为12.9、10.3和7.8nm的MSNs,随后应用三种MSNs包载模型抗原OVA,并考察了MSNs孔径变化对于疫苗体内效率的影响。
结果显示,介孔孔径的改变对于疫苗在淋巴结递送、树突状细胞的摄取及其成熟和活化方面(即DUMPcascade的前三个步骤)并不会产生影响,但在DUMP的第四步:抗原MHCI类提呈的效率却随着介孔孔径的增大而提高,最终导致机体产生细胞免疫应答的强度也随着介孔孔径的增大而增强,其中大孔径的MSNs在无需使用其他佐剂的情况下,即可诱导机体产生有效的细胞免疫应答。让人惊喜的是,以黑色素瘤细胞的细胞裂解液和细胞膜共同作为抗原时,大孔径MSNs可同时高效包载这两类亲疏水性迥异的抗原,并诱导机体产生强效的抗黑色素瘤的细胞免疫应答。
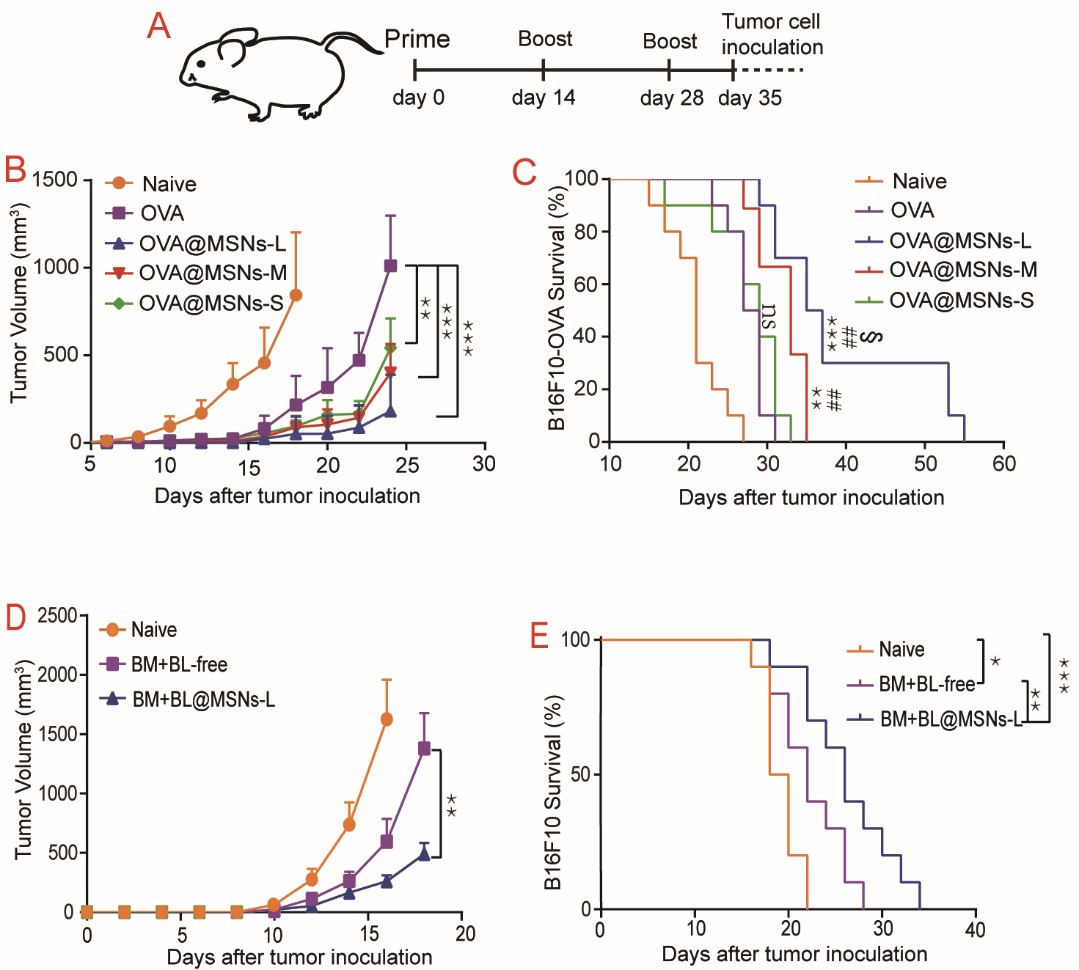
MSNs包载抗原后诱导机体产生抗肿瘤免疫应答
该研究证明通过调节MSNs的孔径可以改变其诱导机体产生免疫应答的能力;同时,MSNs递送肿瘤抗原,诱导机体产生抗肿瘤免疫也证明了MSNs在疫苗递送方面具有很大的发展前景。该研究得到国家自然科学基金杰出青年基金、四川省科技重大专项等项目的资助。
论文全文链接:https://advances.sciencemag.org/content/6/25/eaaz4462/tab-pdf












 微信公众号
微信公众号
 政务微博
政务微博
 头条号
头条号
